Zn+(浓)2H2SO4==ZnS04+SO2↑+2H2O 浓硫酸有强氧化性,他与活泼金属反应不会生成氢气,因为氢气为还原性气体,不会与浓硫酸共存。
反应生成的气体是二氧化硫。
但随着反应进行,硫酸被消耗,其浓度变小,逐渐变成稀硫酸,。
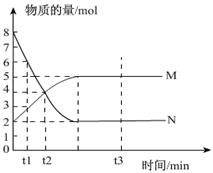
锌和浓硫酸反应方程式:Zn+2H2SO4(浓)==Zn2+ + SO4 2- +SO2↑+2H2O。
锌与浓H2SO4反应可分两个步骤:1、浓硫酸H2SO4Zn+2H2SO4=ZnSo4+SO2↑+2H2O (加热)。
2、随着浓H2SO4的浓度降低 成为稀硫酸 Zn+H2SO4。
浓硫酸和锌反应的 化学 方程式 是什么 一段时间后会产生什么气体 原因是。Zn+(浓)2H2SO4==ZnS04+SO2↑+2H2O ,反应一段时间后会产生氢气,因为硫酸浓度下降,变为稀硫酸
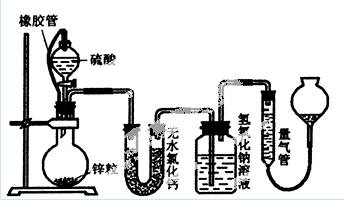
Zn+(浓)2H2SO4==ZnS04+SO2↑+2H2O 亲 记得采纳哦O(∩_∩)O谢谢